Cell重磅! 高脂饮食如何通过慢性代谢压力预激肝脏肿瘤发生?

代谢功能障碍相关脂肪性肝炎(MASH,原名NASH)是当前肝细胞癌(HCC)的主要诱因之一。长期以来,人们普遍认为,慢性肝病通过炎症和基因突变的不断累积,最终推动肿瘤发生。
然而,越来越多的临床证据却显示:在肿瘤真正出现之前,尤其是在非肝硬化阶段,肝细胞并未表现出明显升高的突变负荷。
这提示我们:环境应激(如高脂饮食)诱导的肿瘤发生,可能并非单纯依赖于基因突变的积累。那么,在突变尚未显现之前,肝细胞究竟经历了怎样的状态变化,使其对肿瘤发生变得更加敏感?
日前,来自麻省理工学院的Alex K. Shalek、Ömer H. Yilmaz以及哈佛医学院的Wolfram Goessling团队在Cell上发表了题为“Hepatic adaptation to chronic metabolic stress primes tumorigenesis”的研究论文,提出了“肿瘤预激(tumor priming)”这一关键概念。
研究表明,在长期高脂饮食等慢性代谢压力下,肝细胞并非简单地“受损”,而是通过牺牲核心代谢功能来换取生存优势,逐渐进入一种稳定但具有致癌潜力的预激状态,在肿瘤发生之前悄然重塑肝细胞的状态,使其更容易在未来发生恶性转化。

研究团队构建了一个不依赖基因工程或化学致癌物的高脂饮食(HFD)小鼠模型,完整模拟了从脂肪肝到MASH,再到自发性肝癌的自然过程。通过纵向单细胞测序,研究者追踪了在长期代谢压力下存活下来的肝细胞究竟发生了哪些变化。
结果显示,肝细胞逐渐启动了两类方向相反、但高度协同的变化:
一方面,长期代谢应激会导致肝细胞激活“纵向增加”(Longitudinal Increase)程序,富集了抗凋亡(Bcl2l1)、再生(Cdkn1a)及发育相关基因,这表明细胞为了在恶劣环境中生存,重启了胚胎期的发育程序,以提高生存率;
另一方面,肝细胞启动“纵向减少”(Longitudinal Decrease)程序,显著下调了肝细胞的核心特征基因,如谱系决定因子Hnf4a以及酮体生成限速酶Hmgcs2。这意味着,细胞正在以牺牲专业化功能为代价,换取更强的环境适应能力。
值得注意的是,这种转录状态并非短暂或可逆的应激反应,而是随着代谢压力持续存在而不断加深,提示早期适应性改变与后期肿瘤发生之间存在内在的连续性。
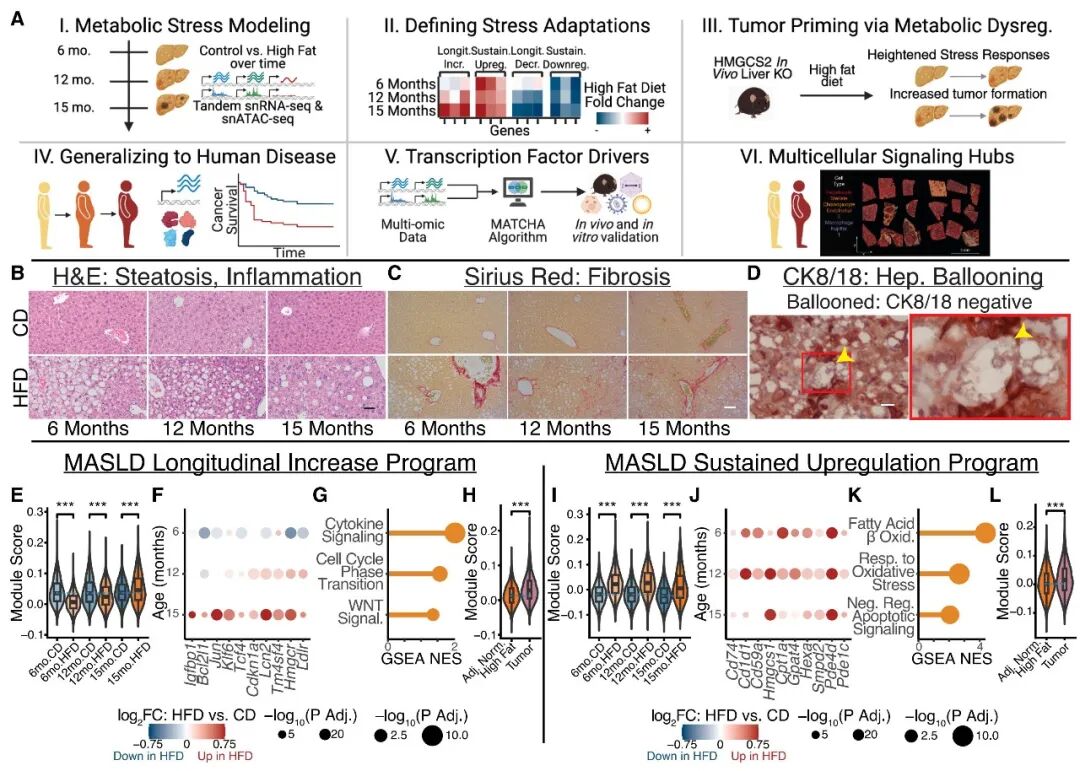
图1. 经历慢性代谢应激的肝细胞的动态响应
为了验证转录组层面的发现,研究团队进行了多模态验证。多重免疫荧光证实,随着HFD时间的延长,肝细胞核内HNF4A蛋白丰度显著降低,而WNT靶基因GLUL的蛋白水平及阳性细胞比例则显著增加。
在HFD喂养15个月时,胆固醇和鞘脂相关的脂质种类显著增加。这一代谢改变与转录组数据高度一致:胆固醇合成限速酶Hmgcr上调,而利用脂质氧化副产物进行酮体生成的限速酶Hmgcs2下调。这一变化意味着肝细胞正在主动关闭高能量输出的代谢通路,以降低自身代谢负荷。
这些结果共同描绘了肝细胞在慢性应激下,从转录到蛋白再到代谢物的全方位功能重塑。
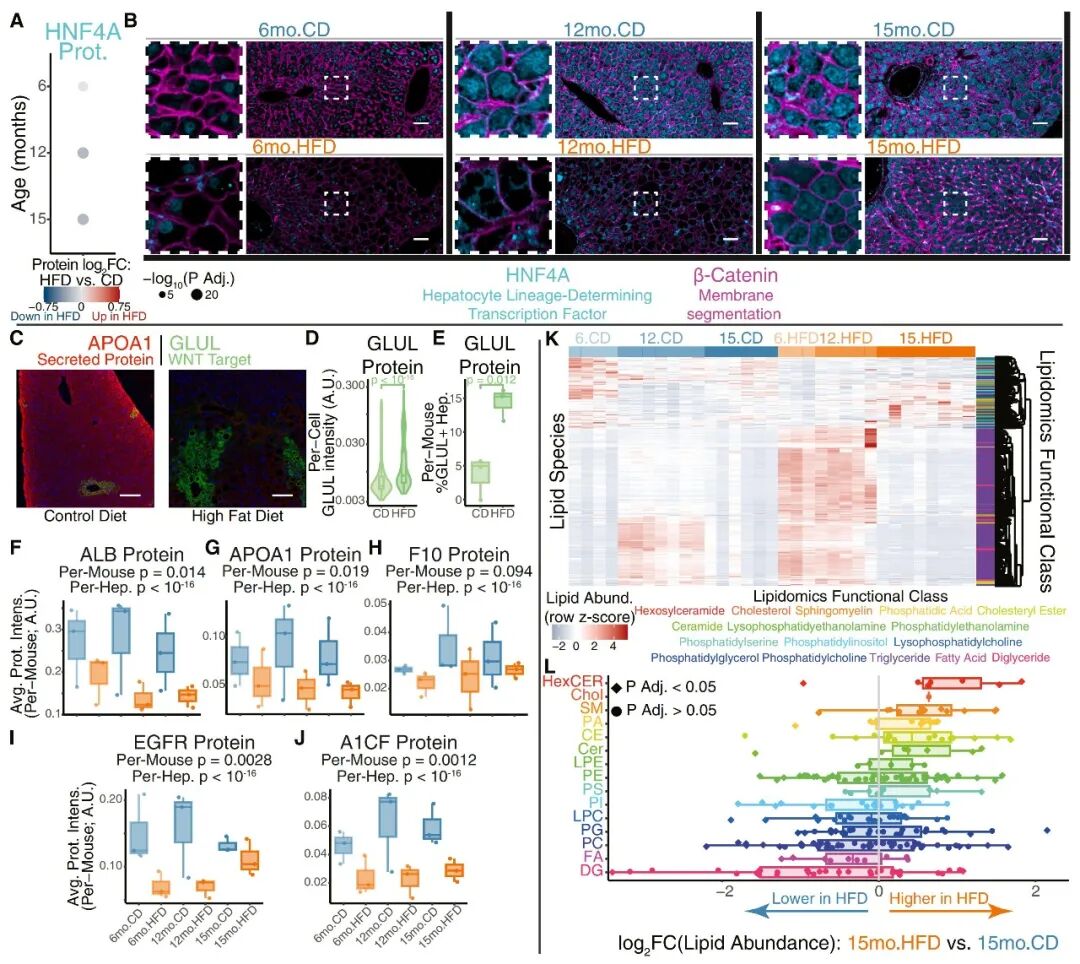
图2. 肝细胞代谢应激反应的多模态验证
为了探究代谢途径的重塑是否直接驱动了应激反应和肿瘤发生,研究团队聚焦于在应激反应中显著下调的酮体生成限速酶HMGCS2。
研究构建了肝脏特异性Hmgcs2敲除小鼠(Hmgcs2 LiverKO),发现在HFD条件下,Hmgcs2的缺失虽然不影响体重和血糖,但显著加剧了肝脏损伤。
单核RNA测序显示,Hmgcs2 LiverKO小鼠的肝细胞在转录状态上明显“提前老化”,其表达谱更接近于长期(12个月)HFD小鼠,表现为发育相关基因更强的上调,以及核心肝功能基因的进一步下调。
更重要的是,在尾静脉注射致癌质粒诱导的HCC模型中,在慢性代谢应激背景下,Hmgcs2的缺失直接导致了肿瘤负荷的显著增加。这有力地证明了代谢酶的下调并非仅仅是疾病的伴随现象,而是通过预激机制主动促进了肿瘤的发生。
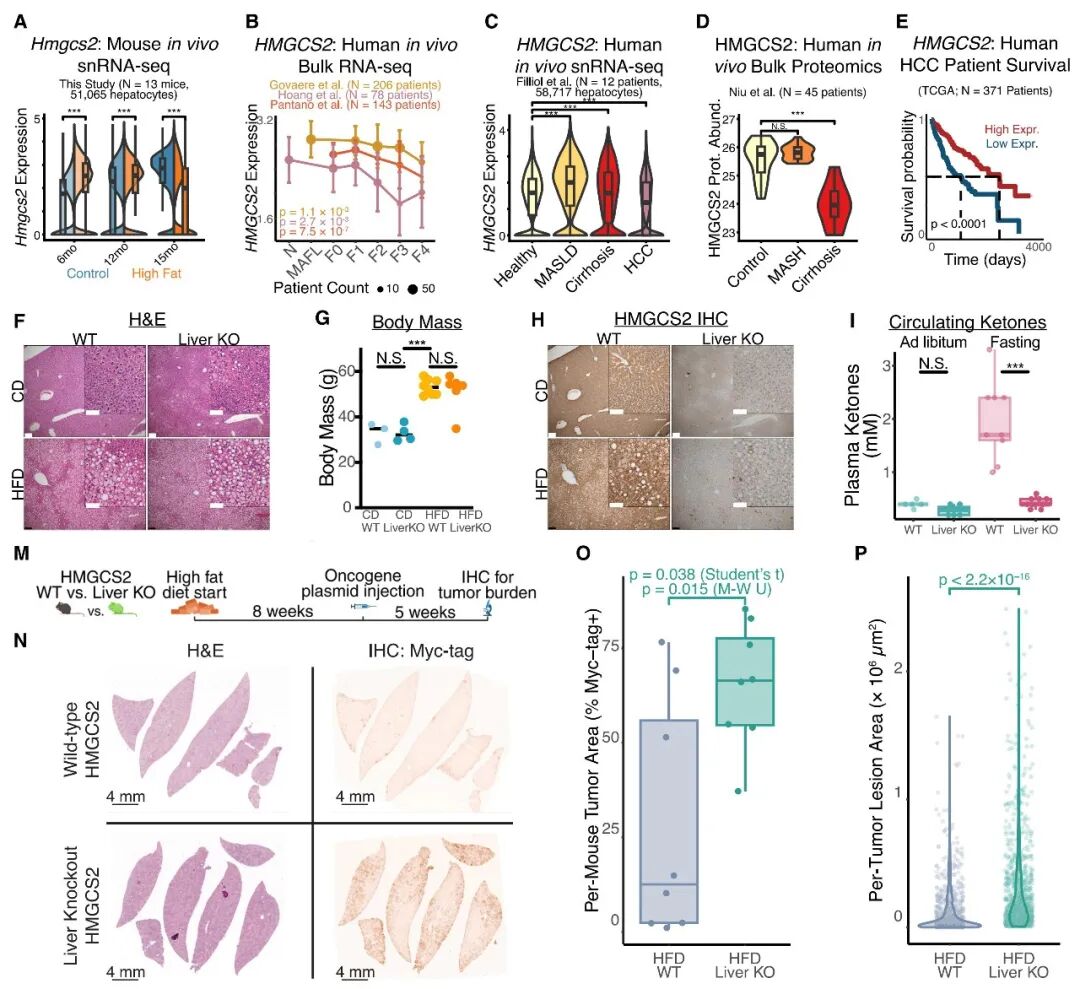
图
为了将小鼠模型中的发现扩展到人类疾病,研究团队分析了多个独立的人类MASH和HCC队列。分析显示,小鼠模型中定义的应激反应程序在人类MASH患者中同样存在,且与疾病进展阶段显著相关。
特别是,“纵向增加”程序在人类HCC中不仅表达上调,而且能够显著分层患者的生存预后,表达该程序的患者生存率显著降低。相反,以HMGCS2为代表的“纵向减少”程序在人类HCC中表达下调,且低表达与不良预后相关。
这些结果表明,肝细胞在慢性代谢应激下形成的这种“生存优先、功能受损”的转录状态,不仅是物种间保守的适应性反应,更是驱动癌症进展和影响临床预后的关键因素。
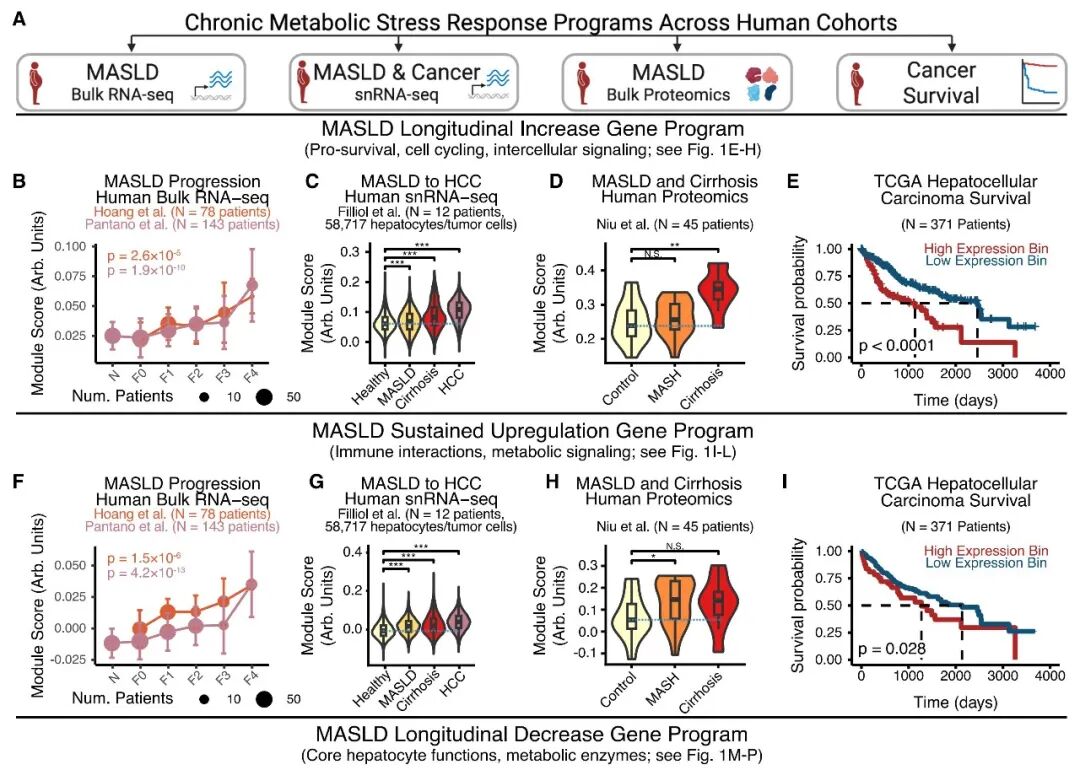
图
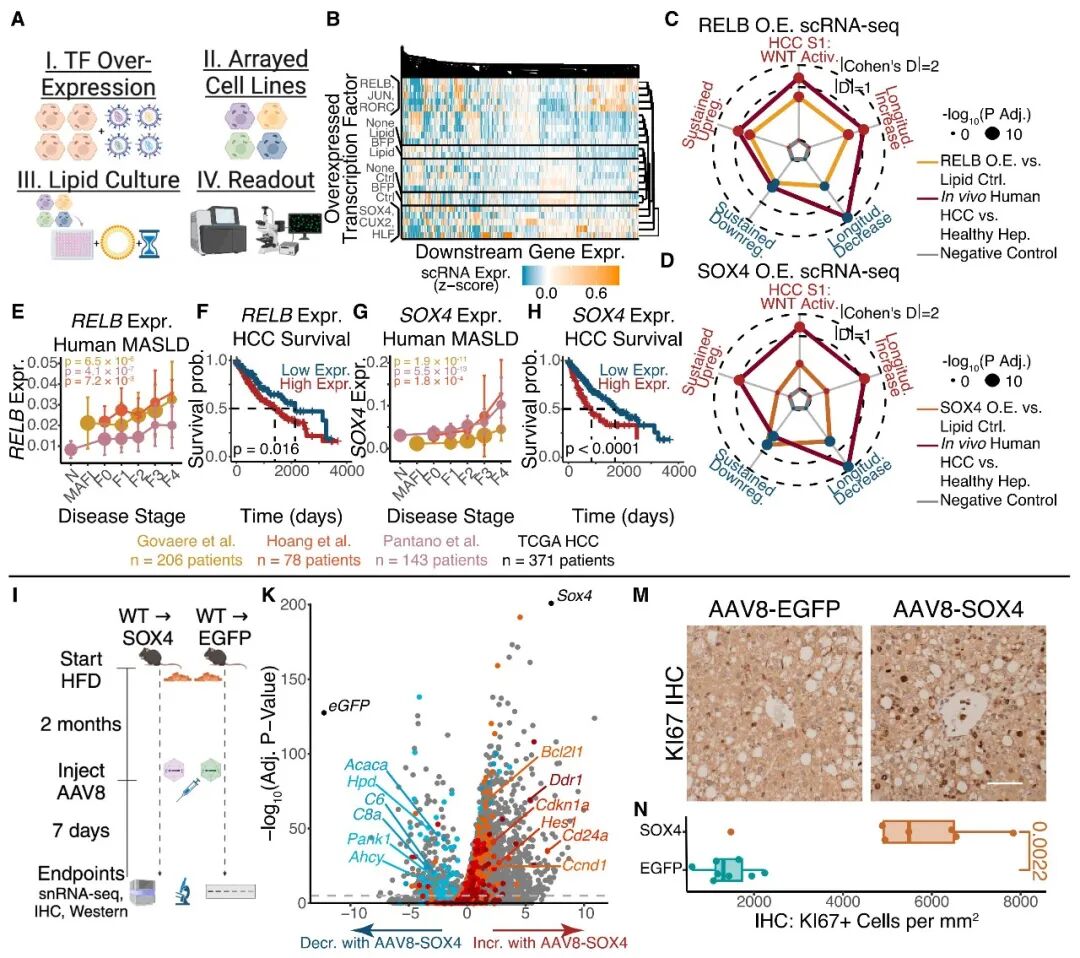
除了代谢酶,转录因子在应激反应中也起着核心作用。研究团队开发了一种名为MATCHA(Multimodal Activity-Transcription Correlation for Hub Analysis)的计算方法,识别出SOX4和RELB是驱动“纵向增加”和“持续上调”程序的关键转录因子。
在体外实验中,过表达SOX4或RELB足以在非肿瘤肝细胞中激活应激反应程序,并增加细胞周期活性。
为了进行体内验证,研究人员利用AAV载体在HFD小鼠肝脏中介导SOX4的过表达。结果显示,SOX4的过表达在体内加速了肝细胞的转录重编程,使其状态向自然病程的晚期(15个月HFD)偏移。
功能上,SOX4过表达直接增加了处于增殖周期的KI67+肝细胞比例,并上调了WNT效应因子β-catenin的水平。
这表明,肝细胞内源性转录因子的异常激活足以在饮食诱导的应激微环境中驱动细胞的可塑性和增殖潜力,为肿瘤发生铺平道路。
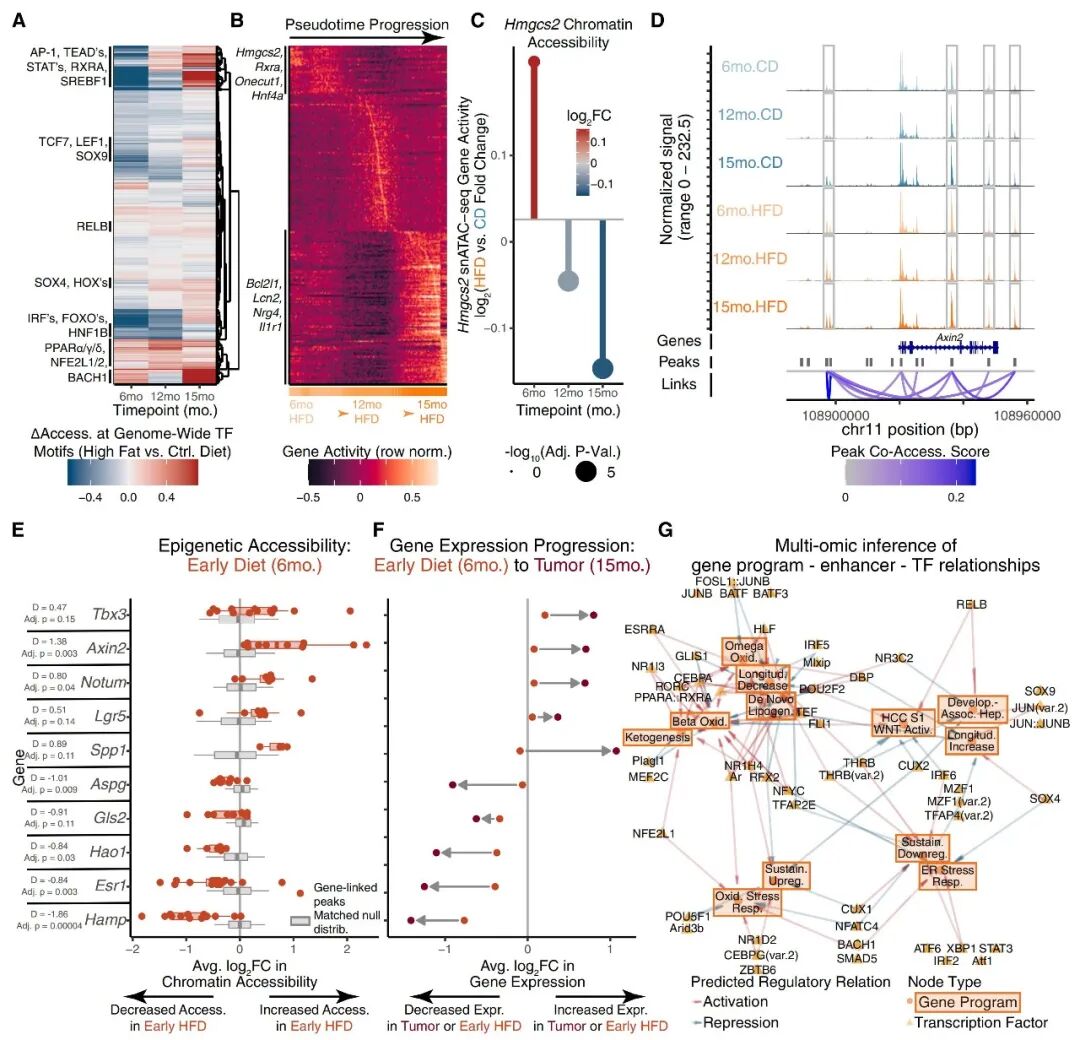
图5. 通过MATCHA算法优先筛选塑造慢性应激反应的关键转录因子
为了解析微环境对肝细胞应激反应的调控,研究团队构建了包含18名受试者的人类MASH肝硬化组织微阵列,并进行了单细胞分辨率的空间转录组测序。研究发现CD9+TREM2+巨噬细胞在空间上与表现出极端应激反应的肝细胞高度共定位。
此外,基因调控空间回归分析揭示了特定的细胞间信号网络:LTB(淋巴毒素β)、JAG1(Notch配体)和IL32被识别为驱动肝细胞“持续上调”和“纵向增加”程序的关键旁分泌信号。特别是,LTB可通过非经典NF-κB通路激活RELB,而RELB和SOX4在空间上也表现出共表达模式。
这揭示了一个由空间结构化微环境信号(如巨噬细胞来源的LTB)→细胞内转录因子(RELB/SOX4)→代谢重塑(HMGCS2下调)共同构成的致癌预激网络。
图
本研究首次系统定义了肝细胞在慢性代谢应激下的适应性重编程轨迹:肝细胞并非被动积累损伤,而是主动通过下调核心代谢功能(如HMGCS2)并激活促存活与发育相关程序(如SOX4、RELB),进入一种长期稳定却具有致癌潜力的预激状态(tumor priming)。
这一状态在肿瘤形成前数月乃至数年即已建立,并依赖于空间免疫微环境的持续输入得以维持。该发现不仅为“非突变性”肿瘤发生机制提供了直接实验证据,也为代谢性肝病患者的早期风险识别和干预靶点选择奠定了理论基础。
云舟生物为本研究提供了用于在C57BL/6小鼠中过表达转录因子SOX4的AAV8病毒载体。
VectorBuilder云舟生物是世界知名分子生物学家蓝田博士创办的基因递送领军企业,在全球设有10余家子公司和办事处,2023年晋升为全球独角兽企业。
云舟生物独创“载体家”平台,开启了个性化基因载体的商品化时代;目前已赋能全球130多个国家和地区,为超过7000家顶尖科研院校和制药公司提供服务,在QS前100高校的客户覆盖率达到了90%,全球TOP30药企的客户覆盖率亦超过90%,产品成果的全球文献引用量逾7000篇。
云舟生物的基因药物CRO、CDMO项目遍布北美、欧洲、日本等多个国家和地区,已成功助力全球数十个项目成功开展IIT或IND研究,其中GMP级别的质粒和慢病毒载体已获得美国FDA的IND正式批准,用于在美国的多中心临床试验。
云舟生物致力于系统性攻克基因递送行业的关键技术瓶颈,为行业和世界创造不可取代的价值。






版权声明
本文仅作者转发或者创作,不代表旺旺头条立场。
如有侵权请联系站长删除
 旺旺头条
旺旺头条






发表评论:
◎欢迎参与讨论,请在这里发表您的看法、交流您的观点。