正源助力 | 祝贺全球首个!创新医疗器械MediBeacon® TGFR获FDA批准
近日,华东医药股份有限公司全资子公司杭州中美华东制药有限公司美国合作方MediBeacon Inc. 对外宣布,其用于评估肾功能的医疗器械MediBeacon® Transdermal GFR System (TGFR)获得美国食品药品监督管理局(FDA)批准。
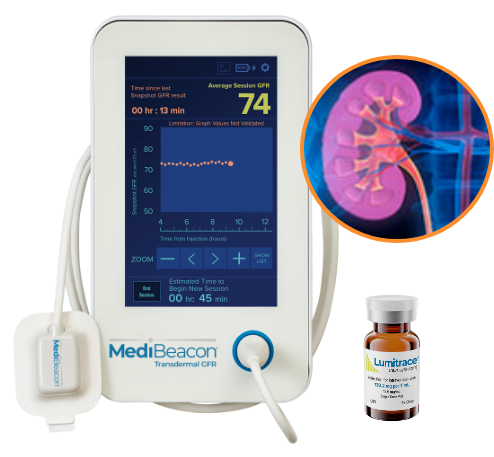
关于MediBeacon® TGFR
MediBeacon® TGFR由监测仪、传感器和Lumitrace®(瑞玛比嗪,Relmapirazin,研发代码:MB-102)注射液(一种非放射性、非碘化荧光GFR示踪剂)组成,旨在通过无创监测外源性示踪剂随时间变化的荧光值来评估肾功能受损或正常的成年患者的肾小球滤过率(GFR),其有效性已在肾功能稳定的患者中得到验证。该系统通过测量荧光示踪剂的体内清除率来评估肾功能,通过放置在皮肤表面的传感器,实时计算经皮测量的Lumitrace®荧光强度相对于时间的变化函数,其所使用的监测方法不受年龄、体重、性别、种族的影响。系统中的传感器每秒可以记录2.5个荧光值,最终TGFR监测仪可以为住院患者或门诊患者提供相应时间段的GFR平均值。TGFR的设计经临床验证可用于床旁评估肾功能稳定的患者的GFR,不需要抽血或尿液分析。目前临床现有的GFR测量方法存在需要多次抽血或留取尿液样本、需要复杂的临床实验室分析,以及无法实现床旁评估等问题。
此产品组合为中美华东与MediBeacon公司合作开发,是全球首个获批用于肾功能正常或受损患者肾功能评估的床旁产品。中美华东拥有该产品在中国大陆、香港、台湾、新加坡、马来西亚等25个亚洲国家或地区的独家商业化权益。2023年7月,该产品的上市前批准(Premarket Approval,PMA)申请获得美国FDA受理。2025年01月17日(美国时间),MediBeacon公司宣布该产品获得美国FDA批准,用于肾功能正常或受损患者的肾功能评估。
本次MediBeacon® TGFR的获批是基于一项在中国和美国开展的验证性Ⅲ期临床试验,即一项MB-102(relmapirazin)及MediBeacon®经皮肾小球滤过率监测系统用于肾功能正常及受损受试者的肾功能评估的关键性、开放标签、多中心、安全性和药代动力学研究(NCT05425719)。该试验招募了具有不同肾功能和不同肤色的受试者,结果显示,临床试验达到主要终点,P30值为94%。P30是GFR估计值落在GFR测量值(mGFR)+/-30%范围内的百分比。

—以上转自华东医药股份有限公司微信公众号

正源助力
军科正源严格遵循国际高标准和规范流程,参与了MB-102(Relmapirazin)注射液境内生产样品生物等效性的临床样本分析,为其申报提供了坚实的数据支撑。
关于军科正源
军科正源药物研究有限责任公司作为拥有引领性科学实力和国际先进检测平台的生物技术药物分析CRO,多年以来一直为广大医药研发企业提供高品质的临床前药代药效评价、药学质量研究和临床样品生物分析检测服务。
军科正源严格遵循ISO/IEC17025、NMPA、EMA、FDA和ICH法规,建立了完善的质量体系,并于2017年2月通过中国合格评定国家认可委员会(CNAS)认证。建立了涵盖小分子化药,蛋白/多肽、单抗及多功能抗体、ADC/PDC、核酸类、疫苗、基因治疗及细胞治疗等全方位生物分析技术集群,解决了各种类型生物技术药物和小分子化药研究的瓶颈问题和关键技术壁垒。
军科正源拥有经验丰富且稳定的技术团队、行业先进的仪器设备,业务范畴涵盖早期药物筛选、生物药CMC质量研究、药代动力学、毒代动力学、药效学、免疫原性、生物标志物、组织病理、药物基因组学等非临床和临床药物评价服务,自2008年团队创建以来,共计为700余家国内外药企的3500多个项目提供了高质量服务,覆盖我国逾70%创新生物制品品种。

版权声明
本文仅作者转发或者创作,不代表旺旺头条立场。
如有侵权请联系站长删除
 旺旺头条
旺旺头条




发表评论:
◎欢迎参与讨论,请在这里发表您的看法、交流您的观点。